La capacitat calorífica d'un gas és la quantitat d'energia que absorbeix un cos quan s'escalfa un grau. Analitzem les principals característiques d'aquesta magnitud física.

Definicions
La calor específica d'un gas és la unitat de massa d'una substància determinada. Les seves unitats de mesura són J/(kg·K). La quantitat de calor que absorbeix el cos en el procés de canviar el seu estat d'agregació s'associa no només amb l'estat inicial i final, sinó també amb el mètode de transició.

Departament
La capacitat calorífica dels gasos es divideix pel valor determinat a volum constant (Cv), pressió constant (Cр).
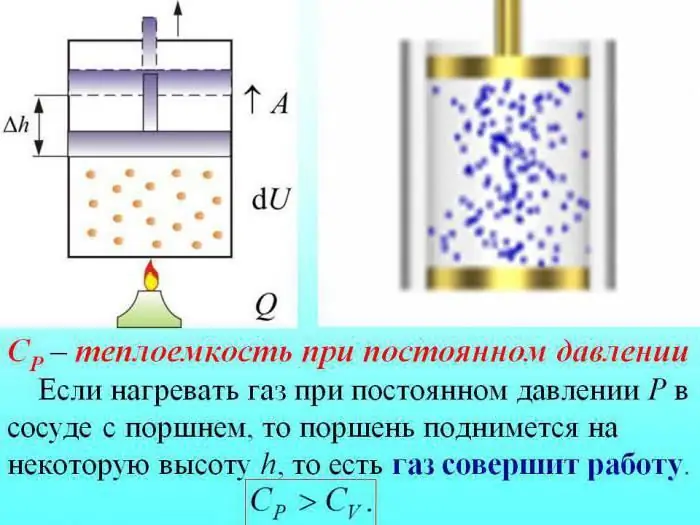
En el cas d'escalfar sense canviar la pressió, es gasta una mica de calor per produir el treball d'expansió del gas i una part de l'energia es gasta per augmentar l'energia interna.
La capacitat calorífica dels gasos a pressió constant ve determinada per la quantitat de calor que es gasta en augmentar l'energia interna.
Estat del gas: característiques, descripció
La capacitat calorífica d'un gas ideal es determina tenint en compte el fet que Сp-Сv=R. Aquesta darrera quantitat s'anomena constant de gas universal. El seu valor correspon a 8,314 J/(mol K).
Quan es realitzen càlculs teòrics de la capacitat calorífica, per exemple, descrivint la relació amb la temperatura, no n'hi ha prou amb utilitzar només mètodes termodinàmics, és important armar-se amb elements de física estàtica.
La capacitat calorífica dels gasos implica el càlcul del valor mitjà de l'energia del moviment de translació d'algunes molècules. Aquest moviment es resumeix a partir del moviment de rotació i translació de la molècula, així com de les vibracions internes dels àtoms.
A la física estàtica, hi ha informació que per a cada grau de llibertat de moviment de rotació i translació, hi ha una quantitat per a un gas que és igual a la meitat de la constant universal del gas.

Dats interessants
Se suposa que una partícula d'un gas monoatòmic té tres graus de llibertat de translació, de manera que la calor específica d'un gas té tres graus de llibertat de translació, dos de rotació i un de vibració. La llei de la seva distribució uniforme condueix a equiparar la calor específica a un volum constant amb R.
Durant els experiments, es va trobar que la capacitat calorífica d'un gas diatòmic correspon al valor R. Aquesta discrepància entre la teoria i la pràctica s'explica pel fet que la capacitat calorífica d'un gas ideal s'associa amb el quàntic efectes, per tant, a l'hora de fer càlculs, és important utilitzar estadístiques basades en quànticsmecànica.
Basat en els fonaments de la mecànica quàntica, qualsevol sistema de partícules que oscil·lin o giren, incloses les molècules de gas, només té alguns valors discrets d'energia.
Si l'energia del moviment tèrmic del sistema no és suficient per excitar oscil·lacions d'una determinada freqüència, aquests moviments no contribueixen a la capacitat calorífica total del sistema.
Com a resultat, un grau de llibertat específic es torna "congelat" i és impossible aplicar-hi la llei d'equipartició.
La capacitat calorífica dels gasos és una característica important de l'estat del qual depèn el funcionament de tot el sistema termodinàmic.
La temperatura a la qual es pot aplicar la llei d'equipartició al grau de llibertat vibracional o rotacional es caracteritza per la teoria quàntica, connecta la constant de Planck amb la constant de Boltzmann.

Gasos diatòmics
Els espais entre els nivells d'energia de rotació d'aquests gasos són d'un petit nombre de graus. L'excepció és l'hidrogen, en què el valor de la temperatura està determinat per centenars de graus.
És per això que la capacitat calorífica d'un gas a pressió constant és difícil de descriure per la llei de la distribució uniforme. En l'estadística quàntica, a l'hora de determinar la capacitat calorífica, es té en compte que la seva part vibratòria, en el cas d'una disminució de la temperatura, disminueix ràpidament i arriba a zero.
Aquest fenomen explica el fet que a temperatura ambient pràcticament no hi ha part vibratòria de la capacitat calorífica, pergas diatòmic, correspon a la constant R.
La capacitat calorífica d'un gas a volum constant en el cas d'indicadors de baixa temperatura es determina mitjançant estadístiques quàntiques. Hi ha el principi de Nernst, que s'anomena tercera llei de la termodinàmica. Segons la seva formulació, la capacitat calorífica molar d'un gas disminuirà amb la disminució de la temperatura, tendint a zero.

Característiques dels sòlids
Si la capacitat calorífica d'una mescla de gasos es pot explicar mitjançant l'estadística quàntica, aleshores per a un estat sòlid d'agregació, el moviment tèrmic es caracteritza per lleugeres fluctuacions de partícules prop de la posició d'equilibri.
Cada àtom té tres graus de llibertat vibracional, per tant, d'acord amb la llei d'equipartició, la capacitat calorífica molar d'un sòlid es pot calcular com 3nR, sent n el nombre d'àtoms d'una molècula.
A la pràctica, aquest nombre és el límit al qual tendeix la capacitat calorífica d'un cos sòlid a altes temperatures.
Es pot obtenir el màxim a temperatures normals per a alguns elements, inclosos els metalls. Per a n=1, es compleix la llei de Dulong i Petit, però per a substàncies complexes és bastant difícil assolir aquest límit. Com que el límit no es pot obtenir en realitat, es produeix la descomposició o la fusió del sòlid.
Història de la teoria quàntica
Els fundadors de la teoria quàntica són Einstein i Debye a principis del segle XX. Es basa en la quantificació dels moviments oscil·latoris dels àtoms en un determinatcristall. En el cas dels indicadors de baixa temperatura, la capacitat calorífica d'un cos sòlid resulta ser directament proporcional al valor absolut pres al cub. Aquesta relació s'ha anomenat llei de Debye. Com a criteri que permet distingir entre indicadors de temperatura baixa i alta, es pren la seva comparació amb la temperatura de Debye.
Aquest valor està determinat per l'espectre de vibracions d'un àtom al cos, per tant depèn seriosament de les característiques de la seva estructura cristal·lina.
QD és un valor que té diversos centenars de K, però, per exemple, és molt més alt en diamant.
Els electrons de conducció contribueixen significativament a la capacitat calorífica dels metalls. Per calcular-ho, s'utilitzen les estadístiques quàntiques de Fermi. La conductivitat electrònica dels àtoms metàl·lics és directament proporcional a la temperatura absoluta. Com que és un valor insignificant, només es té en compte a temperatures que tendeixen al zero absolut.
Mètodes per determinar la capacitat calorífica
El principal mètode experimental és la calorimetria. Per realitzar un càlcul teòric de la capacitat calorífica s'utilitza la termodinàmica estadística. És vàlid per a un gas ideal, així com per a cossos cristal·lins, es realitza a partir de dades experimentals sobre l'estructura de la matèria.
Els mètodes empírics per calcular la capacitat calorífica d'un gas ideal es basen en la idea de l'estructura química, la contribució de grups individuals d'àtoms a Ср.
Per als líquids, també s'utilitzen mètodes que es basen en l'ús de la termodinàmicacicles que permeten passar de la capacitat calorífica d'un gas ideal a un líquid mitjançant la derivada de la temperatura de l'entalpia del procés d'evaporació.
En el cas d'una solució, no es permet el càlcul de la capacitat calorífica com a funció additiva, ja que l'excés de valor de la capacitat calorífica de la solució és bàsicament significatiu.
Per avaluar-ho, necessitem la teoria estadística molecular de les solucions. El més difícil és la identificació de la capacitat calorífica de sistemes heterogenis en l'anàlisi termodinàmica.

Conclusió
L'estudi de la capacitat calorífica permet calcular el balanç energètic dels processos que es produeixen en reactors químics, així com en altres aparells de producció química. A més, aquest valor és necessari per seleccionar els tipus òptims de refrigerants.
En l'actualitat, la determinació experimental de la capacitat calorífica de les substàncies per a diferents intervals de temperatura -des de valors baixos fins a valors alts- és l'opció principal per determinar les característiques termodinàmiques d'una substància. Quan es calcula l'entropia i l'entalpia d'una substància, s'utilitzen integrals de capacitat calorífica. La informació sobre la capacitat calorífica dels reactius químics en un interval de temperatura determinat us permet calcular l'efecte tèrmic del procés. La informació sobre la capacitat calorífica de les solucions permet calcular els seus paràmetres termodinàmics a qualsevol valor de temperatura dins de l'interval analitzat.
Per exemple, un líquid es caracteritza per la despesa d'una part de la calor per canviar el valor de l'energia potencialmolècules que reaccionen. Aquest valor s'anomena capacitat calorífica de "configuració", que s'utilitza per descriure les solucions.
És difícil realitzar càlculs matemàtics complets sense tenir en compte les característiques termodinàmiques d'una substància, el seu estat d'agregació. És per això que per als líquids, gasos, sòlids s'utilitza una característica com la capacitat calorífica específica, que permet caracteritzar els paràmetres energètics d'una substància.






