Quan s'estudia el comportament dels gasos en física, es presta molta atenció als isoprocessos, és a dir, aquestes transicions entre els estats del sistema, durant les quals es conserva un paràmetre termodinàmic. Tanmateix, hi ha una transició de gas entre estats, que no és un isoprocés, però que té un paper important en la natura i la tecnologia. Aquest és un procés adiabàtic. En aquest article, ho analitzarem amb més detall, centrant-nos en quin és l'exponent adiabàtic del gas.
Procés adiabàtic
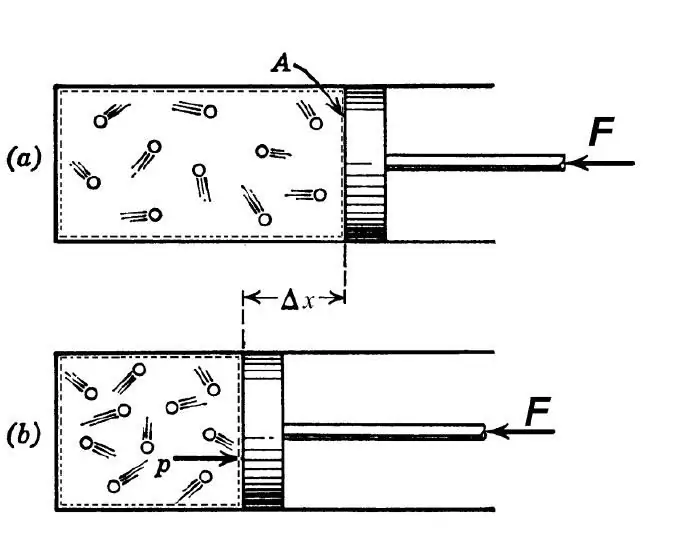
Segons la definició termodinàmica, s'entén per procés adiabàtic com una transició entre els estats inicial i final del sistema, com a conseqüència de la qual no hi ha intercanvi de calor entre l'entorn extern i el sistema objecte d'estudi. Aquest procés és possible amb les dues condicions següents:
- conductivitat tèrmica entre el medi extern iel sistema és baix per un motiu o un altre;
- la velocitat del procés és alta, de manera que l'intercanvi de calor no té temps per produir-se.
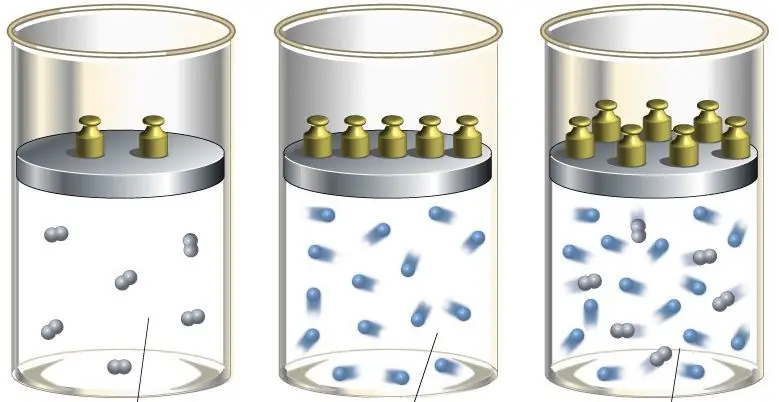
En enginyeria, la transició adiabàtica s'utilitza tant per escalfar el gas durant la seva forta compressió com per refredar-lo durant la ràpida expansió. A la natura, la transició termodinàmica en qüestió es manifesta quan una massa d'aire puja o baixa per un vessant. Aquests pujades i baixades provoquen un canvi en el punt de rosada de l'aire i les precipitacions.
Equació de Poisson per al gas ideal adiabàtic

Un gas ideal és un sistema en què les partícules es mouen aleatòriament a altes velocitats, no interaccionen entre elles i són adimensionals. Aquest model és molt senzill pel que fa a la seva descripció matemàtica.
Segons la definició de procés adiabàtic, l'expressió següent es pot escriure d'acord amb la primera llei de la termodinàmica:
dU=-PdV.
En altres paraules, un gas, en expansió o contracció, funciona PdV a causa d'un canvi corresponent en la seva energia interna dU.
En el cas d'un gas ideal, si fem servir l'equació d'estat (llei de Clapeyron-Mendeleev), podem obtenir l'expressió següent:
PVγ=const.
Aquesta igu altat s'anomena equació de Poisson. Les persones familiaritzades amb la física dels gasos notaran que si el valor de γ és igual a 1, aleshores l'equació de Poisson entrarà en la llei de Boyle-Mariotte (isotèrmica).procés). Tanmateix, aquesta transformació de les equacions és impossible, ja que γ per a qualsevol tipus de gas ideal és més gran que un. La quantitat γ (gamma) s'anomena índex adiabàtic d'un gas ideal. Fem una ullada més de prop al seu significat físic.
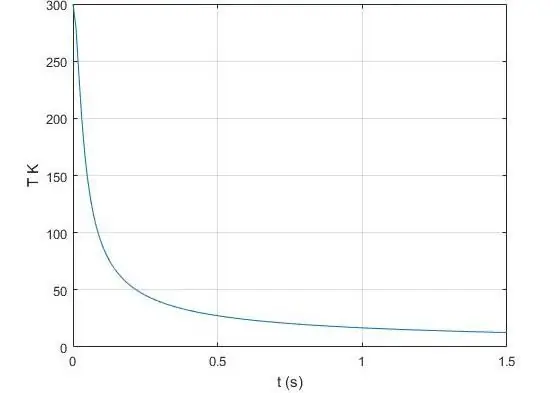
Quin és l'exponent adiabàtic?
L'exponent γ, que apareix a l'equació de Poisson per a un gas ideal, és la relació entre la capacitat calorífica a pressió constant i el mateix valor, però ja a volum constant. En física, la capacitat calorífica és la quantitat de calor que s'ha de transferir o prendre d'un sistema determinat perquè canviï la seva temperatura en 1 Kelvin. Denotarem la capacitat calorífica isobàrica amb el símbol CP, i la capacitat isocòrica amb el símbol CV. Aleshores la igu altat és vàlida per a γ:
γ=CP/CV.
Com que γ és sempre més gran que un, mostra quantes vegades la capacitat calorífica isobàrica del sistema de gas estudiat supera la característica isòcòrica similar.
Capacitat calorífica de CP i CV
Per determinar l'exponent adiabàtic, cal tenir una bona comprensió del significat de les magnituds CP i CV. Per fer-ho, realitzarem el següent experiment mental: imagineu que el gas es troba en un sistema tancat en un recipient amb parets sòlides. Si s'escalfa el recipient, aleshores tota la calor comunicada es convertirà idealment en energia interna del gas. En aquesta situació, la igu altat serà vàlida:
dU=CVdT.
ValorCV defineix la quantitat de calor que s'ha de transferir al sistema per tal d'escalfar-lo isocòricamente en 1 K.
Ara suposem que el gas està en un recipient amb un pistó en moviment. En el procés d'escalfament d'aquest sistema, el pistó es mourà, assegurant que es mantingui una pressió constant. Com que l'entalpia del sistema en aquest cas serà igual al producte de la capacitat calorífica isobàrica i el canvi de temperatura, la primera llei de la termodinàmica prendrà la forma:
CPdT=CVdT + PdV.
A partir d'aquí es pot veure que CP>CV, ja que en el cas d'un canvi isobàric d'estats cal gastar calor no només per augmentar la temperatura del sistema, i per tant la seva energia interna, sinó també el treball realitzat pel gas durant la seva expansió.
El valor de γ per a un gas monoatòmic ideal
El sistema de gas més senzill és un gas ideal monoatòmic. Suposem que tenim 1 mol d'aquest gas. Recordeu que en el procés d'escalfament isobàric d'1 mol de gas només en 1 Kelvin, funciona igual a R. Aquest símbol s'utilitza habitualment per indicar la constant de gas universal. És igual a 8.314 J / (molK). Aplicant l'última expressió del paràgraf anterior per a aquest cas, obtenim la següent igu altat:
CP=CV+ R.
Des d'on podeu determinar el valor de la capacitat calorífica isocòrica CV:
γ=CP/CV;
CV=R/(γ-1).
Se sap que per un lunargas monoatòmic, el valor de la capacitat calorífica isocòrica és:
CV=3/2R.
De les dues últimes igu altats segueix el valor de l'exponent adiabàtic:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Tingueu en compte que el valor de γ depèn únicament de les propietats internes del propi gas (de la naturalesa poliatòmica de les seves molècules) i no depèn de la quantitat de substància del sistema.
Dependència de γ del nombre de graus de llibertat
L'equació de la capacitat calorífica isocòrica d'un gas monoatòmic s'ha escrit més amunt. El coeficient 3/2 que hi apareixia està relacionat amb el nombre de graus de llibertat d'un àtom. Té la capacitat de moure's només en una de les tres direccions de l'espai, és a dir, només hi ha graus de llibertat de translació.
Si el sistema està format per molècules diatòmiques, s'afegeixen dos graus de rotació més als tres de translació. Per tant, l'expressió per a CV es converteix en:
CV=5/2R.
Llavors el valor de γ serà:
γ=7/5=1, 4.
Tingueu en compte que la molècula diatòmica en realitat té un grau de llibertat vibracional més, però a temperatures de diversos centenars de Kelvin no s'activa i no contribueix a la capacitat calorífica.
Si les molècules de gas consten de més de dos àtoms, tindran 6 graus de llibertat. L'exponent adiabàtic en aquest cas serà igual a:
γ=4/3 ≈ 1, 33.
Així doncsAixí, a mesura que augmenta el nombre d'àtoms d'una molècula de gas, el valor de γ disminueix. Si construïu un gràfic adiabàtic en els eixos P-V, notareu que la corba d'un gas monoatòmic es comportarà de manera més clara que la d'un gas poliatòmic.
Exponent adiabàtic per a una barreja de gasos
A d alt hem demostrat que el valor de γ no depèn de la composició química del sistema de gas. Tanmateix, depèn del nombre d'àtoms que formen les seves molècules. Suposem que el sistema consta de N components. La fracció atòmica del component i de la mescla és ai. Aleshores, per determinar l'exponent adiabàtic de la mescla, podeu utilitzar l'expressió següent:
γ=∑i=1N(aiγ i).
On γi és el valor γ per al component i-è.
Per exemple, aquesta expressió es pot utilitzar per determinar la γ de l'aire. Com que està format per un 99% de molècules diatòmiques d'oxigen i nitrogen, el seu índex adiabàtic hauria d'estar molt proper al valor d'1,4, cosa que es confirma amb la determinació experimental d'aquest valor.






