El mètode d'anàlisi conductomètric és la mesura de la conductivitat electrolítica per controlar el progrés d'una reacció química. Aquesta ciència s'aplica àmpliament a la química analítica, on la valoració és un mètode d'operació estàndard. Què és la conductometria? En la pràctica habitual en química analítica, el terme s'utilitza com a sinònim de valoració, mentre que també s'utilitza per descriure aplicacions que no són de valoració. Quin és l'avantatge d'utilitzar aquest mètode d'anàlisi? Sovint s'utilitza per determinar la conductivitat global d'una solució o per analitzar el punt final d'una valoració amb ions.
Història
Les mesures de conductivitat van començar ja al segle XVIII, quan Andreas Baumgartner va notar que les aigües salades i minerals de Bad Gastein aÀustria condueix l'electricitat. Així, l'ús d'aquest mètode per determinar la puresa de l'aigua, que s'utilitza sovint avui per provar l'efectivitat dels sistemes de purificació d'aigua, va començar el 1776. Així va començar la història del mètode d'anàlisi conductomètric.
Friedrich Kohlrausch va continuar el desenvolupament d'aquesta ciència a la dècada de 1860, quan va aplicar el corrent altern a l'aigua, àcids i altres solucions. Al voltant d'aquesta època, Willis Whitney, que estava estudiant les interaccions dels complexos d'àcid sulfúric i sulfat de crom, va trobar el primer punt final conductomètric. Aquestes troballes van culminar amb la valoració potenciomètrica i el primer instrument per a l'anàlisi volumètrica de Robert Behrend el 1883 en la valoració de clorur i bromur HgNO3. Per tant, el mètode d'anàlisi conductomètric modern es basa en Behrend.
Aquest desenvolupament va permetre provar la solubilitat de les sals i la concentració d'ions d'hidrogen, així com les titulacions àcid-base i redox. El mètode d'anàlisi conductomètric es va millorar amb el desenvolupament de l'elèctrode de vidre, que va començar l'any 1909.
Titració
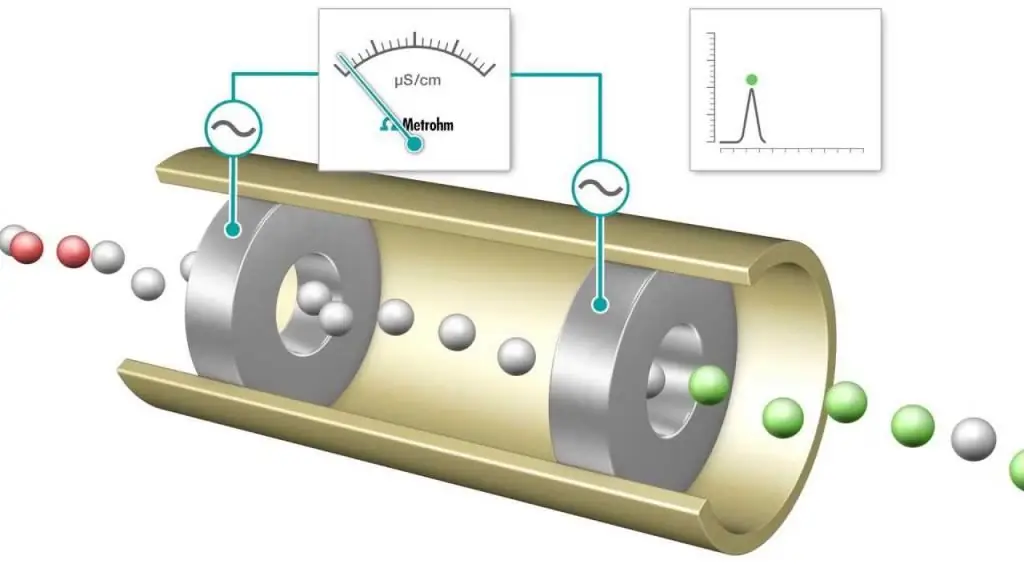
La valoració conductomètrica és una mesura en què la conductivitat electrolítica d'una mescla de reacció es controla contínuament afegint un reactiu. El punt d'equivalència és el punt en què la conductivitat canvia sobtadament. Un augment o disminució notable de la conductivitat s'associa amb un canvi en la concentració dels dos ions més conductors, els ions hidrogen i hidròxid. Aquest mètodees pot utilitzar per valorar solucions de colors o suspensió homogènia (per exemple, suspensió de pasta de fusta) que no es poden utilitzar amb indicadors convencionals.
Sovint es realitzen valoracions àcid-base i redox, que utilitzen indicadors comuns per determinar el punt final, com ara taronja de metil, fenolftaleïna per a la valoració àcid-base i solucions de midó per a un procés redox de tipus iodomètric. Tanmateix, les mesures de conductivitat elèctrica també es poden utilitzar com a eina per determinar el punt final, per exemple quan s'observa una solució d'HCl amb la base forta NaOH.
Neutralització de protons
A mesura que avança la valoració, els protons es neutralitzen per formar NaOH formant aigua. Per cada quantitat de NaOH afegit, s'elimina un nombre equivalent d'ions d'hidrogen. En efecte, el catió H+ mòbil es substitueix per l'ió Na+ menys mòbil, i la conductivitat de la solució titulada, així com la conductivitat cel·lular mesurada, disminueix. Això continua fins que s'arriba a un punt d'equivalència en el qual es pot obtenir una solució de clorur de sodi NaCl. Si s'afegeix més base, hi ha un augment a mesura que s'afegeixen més ions Na+ i OH- i la reacció de neutralització ja no elimina una quantitat apreciable d'H+.

En conseqüència, quan es titula un àcid fort amb una base forta, la conductivitat té un mínim en el punt d'equivalència. Aquest mínimes pot utilitzar en lloc d'un colorant indicador per determinar el punt final d'una titulació. La corba de valoració és un gràfic dels valors mesurats de conductivitat o conductivitat en funció del volum de solució de NaOH afegit. La corba de valoració es pot utilitzar per determinar gràficament el punt d'equivalència. El mètode d'anàlisi conductomètric (i el seu ús) és extremadament rellevant en la química moderna.
Reacció
Per a una reacció entre una base àcid feble i feble, la conductivitat elèctrica primer disminueix una mica, ja que s'utilitzen pocs ions H+ disponibles. Aleshores, la conductivitat augmenta lleugerament fins al volum del punt d'equivalència a causa de l'aportació del catió de la sal i de l'anió (aquesta contribució en el cas d'una base àcida forta és insignificant i no s'hi considera). Després d'arribar al punt d'equivalència, la conductivitat augmenta ràpidament a causa d'un excés d'ions OH.
Els detectors de conductivitat (mètode d'anàlisi conductomètric) també s'utilitzen per mesurar concentracions d'electròlits en solucions aquoses. La concentració molar de l'analit que crea la conductivitat de la solució es pot obtenir a partir de la resistència elèctrica mesurada de la solució.
Mètode d'anàlisi conductomètric: principi i fórmules
(2.4.13) C=Constcell1Λm1Res, on Constcell és un valor constant en funció de la cèl·lula de mesura, Res és la resistència elèctrica mesurada pel dispositiu (segons la llei d'Ohm Res=I / V, i amb una constant tensió V mesura I intensitat permet calcular Res), i Λm és l'equivalentconductivitat de les partícules iòniques. Encara que per a finalitats pràctiques Λm es pot considerar constant, depèn de la concentració segons la llei de Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, on Θ és una constant i Λm0 és la característica de conductivitat molar limitant de cada ió. La conductivitat molar, al seu torn, depèn de la temperatura.
Scrit
El desenvolupament del mètode conductomètric d'anàlisi de mesura ha portat els científics a nous descobriments. Els científics van determinar la relació de sobresaturació crítica, Scrit, utilitzant conductometria en un sistema homogeni de precipitació AgCl en excés d'ions Ag +, utilitzant la hidròlisi de clorur d'alquil com a font d'ions CI". Van trobar Script=1,51, 1,73 i 1,85 a 15, 25 i 35 °C respectivament, on S=([Ag+][Cl-] / Ksp) 1/2 segons la seva definició. Si aquesta definició del factor de sobresaturació es converteix a la nostra (S=[Ag+][Cl-] / Ksp), els resultats són 2,28, 2,99 i 3,42, respectivament, d'acord força bé amb els resultats del present estudi. Tanmateix, la dependència de la temperatura de Scrit és oposada a la descrita en el present estudi. Tot i que la raó d'aquesta contradicció no està clara, la disminució de Scrit amb l'augment de la temperatura pot ser força raonable, ja que la velocitat de nucleació canvia dràsticament amb un petit canvi en ΔGm/ kT i, per tant, en ΔGm/ kT, que és proporcional a T − 3 (lnSm) 2 segons la fórmula (1.4.12) es considera gairebé constant amb el canvi de temperatura en el sistema donat. Per cert, la definició de S ha de ser [Ag +] [Cl -] / Ksp, ja que la relació de sobresaturació en termes deLa concentració de monòmers [AgCl] es dóna inicialment com S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka i Iwasaki
La història del mètode d'anàlisi conductomètric va ser continuada per dos científics japonesos emblemàtics. Tanaka i Iwasaki van estudiar el procés de nucleació de partícules AgCl i AgBr mitjançant el mètode de flux aturat en combinació amb un espectrofotòmetre multicanal, que és útil per estudiar un procés ràpid de l'ordre del msec. Van trobar que algun complex específic d'halogenur de plata AgXm (m-1), amb una banda d'absorció UV força estreta, es va formar instantàniament quan es va barrejar una solució d'AgC104 de l'ordre de 10-4 mol dm-3 amb un KX (X=Cl o Br) solució de l'ordre de 10-2 a 10-1 mol dm-3 seguida de la seva ràpida desintegració d'uns 10 ms amb la formació d'un producte intermedi amb una àmplia absorció UV i un canvi molt més lent en l'espectre. del producte intermedi. Van interpretar l'intermedi com a nuclis monodispersos (AgX) n formats per n molècules i van determinar n a partir de la relació aparent -dC/dt α Cn a t=0 per a diverses concentracions inicials de C precursor AgXm (m-1) - (n=7). -10 per a AgCl, n=3-4 per a AgBr).

No obstant això, com que el precursor AgXm (m − 1) decau de manera no estacionària, la teoria de la nucleació quasi estacionària no s'aplica en aquest procés i, per tant, el valor resultant de n no es correspon amb el nvalor dels nuclis crítics. Si el producte intermedi conté nuclis monodispersos n,format pel complex monomèric, és possible que la relació -dC/dt α C no es mantingui. A menys que suposem que els grups més petits que n-mers estan en equilibri, ki − 1, ici − 1c1=ki, i − 1ci, entre si en una reacció seqüencial c1 → c2 → c3 →… → cn − 1 → cn., i només l'últim pas cn − 1 → cn és irreversible; és a dir, c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
A més, s'ha de suposar que les concentracions de cúmuls de 2 a n-1 tenen concentracions d'equilibri insignificants. Tanmateix, sembla que no hi ha cap base per justificar aquestes suposicions. D' altra banda, hem intentat calcular els radis dels nuclis crítics i els coeficients de sobresaturació S al final del procés ràpid, utilitzant γ=101 mJ m - 2 per a AgCl19 cúbic i γ=109 mJ m - 2 per a AgBr20 cúbic, suposant que els valors de n, 7-10 per a AgCl19 i 3-4 per a AgBr20, són equivalents a la mida dels nuclis monodispersos, n. El mètode d'anàlisi conductomètric, les revisions dels quals van des de la simple aprovació fins a l'admiració, va donar un nou naixement a la química com a ciència.
Com a resultat, els científics van descobrir la fórmula següent: r=0,451 nm i S=105 per a AgCl amb n=9; r=0,358 nm i S=1230 per a AgBr amb n=4. Atès que els seus sistemes són comparables als de Davis i Jones, que van obtenir una sobresaturació crítica d'AgCl d'uns 1,7-2,0 a 25 °C. Utilitzant conductometria de mescla directa en volums iguals de solucions aquoses diluïdes d'AgNO3 i KCl, és possible que els valors de S extremadament alts no reflecteixin factors de sobresaturació reals.en equilibri amb nuclis intermedis.
absorció UV
Sembla més raonable atribuir un intermedi amb una àmplia absorció UV a nuclis molt més grans que la mitjana amb una àmplia distribució de mida generada per una reacció seqüencial no estacionària. El canvi lent posterior dels nuclis intermedis sembla estar relacionat amb la seva maduració a Ostwald.

En el context anterior, el químic nord-americà Nielsen també va derivar una nsimilar al voltant de 12 i una S corresponent superior a 103 per a la nucleació de partícules de sulfat de bari a partir de mesures de terbolesa en funció de la sobresaturació, utilitzant n=dlogJ / dlogC en una teoria semblant a Becher-Dering a la fórmula. (1.3.37), però donant (n+ 1) en lloc de n. Com que les solucions d'ions bari i ions sulfat es van barrejar directament en aquest experiment, la nucleació transitòria ràpida hauria d'haver acabat immediatament després de la barreja, i el que es va mesurar podria ser la velocitat de maduració i/o fusió posterior lenta d'Ostwald dels nuclis generats. Aparentment, aquesta és la raó del valor poc raonable de n i la supersaturació extremadament alta. Per tant, hem de tornar a assenyalar que sempre és necessari algun reservori d'espècies monomèriques que les alliberi en resposta al seu consum per aconseguir una nucleació quasi estacionària en un sistema tancat. Totes les teories clàssiques de la nucleació, inclosa la teoria de Becher-Döring, assumeixen implícitament aquesta condició. Definició de conductometriaEl mètode d'anàlisi es va donar a les seccions de l'article anterior.
Altres científics han investigat el procés de nucleació transitòria d'halogenur de plata per radiòlisi polsada d'aigua que conté halogenur de metilè i ions de plata, durant el qual l'halogenur de metilè es descomposa per alliberar ions d'halogenur per electrons hidratats generats per radiació polsada en el rang. de 4 ns a 3 μs. Els espectres dels productes es van registrar mitjançant un fotomultiplicador i una càmera de ratlles i es va trobar que els precursors d'halogenur de plata monomèrics es formaven al llarg d'un temps de l'ordre de microsegons seguits d'un procés de nucleació similar al observat per Tanaka i Iwasaki. Els seus resultats mostren clarament que el procés de nucleació dels halogenurs de plata per mescla directa dels reactius consta de dues etapes elementals; és a dir, la formació d'un precursor monomèric de l'ordre de μs i la posterior transició a nuclis de l'ordre de 10 ms. Cal tenir en compte que la mida mitjana dels nuclis és d'uns 10 nm.
Saturació
Pel que fa als coeficients de sobresaturació per a la nucleació de partícules d'AgCl en sistemes oberts en què s'introdueixen contínuament altes concentracions de reactius com AgNO3 i KCl a la solució de gelatina durant tota la precipitació, Strong i Wey31 van informar 1,029 (80 ° C) - 1,260 (40 ° C) i Leubner32 van informar 1,024 a 60 ° C, segons s'estima a partir de la mesura de la taxa de creixement de les partícules de llavors d'AgCl a una sobresaturació crítica. Aquesta és l'essència del mètode conductomètric d'anàlisi quantitativa.
D' altra banda, per a sistemes oberts de partícules AgBr, algunsvalors estimats del coeficient de sobresaturació crític, Script: Scrit∼- 1,5 a 70 °C segons Wey i Strong33 a partir de la taxa de creixement màxima depenent de la mida determinada en trobar el llindar de renucleació a diferents velocitats d'afegir una solució d'AgNO3 a un KBr solució en presència de partícules de llavors mitjançant els dobles dolls; Script=1,2-1,5 a 25 °C segons Jagannathan i Wey34 com a factor de sobresaturació màxim determinat a partir de l'equació de Gibbs-Thomson amb les seves dades sobre la mida mitjana mínima dels nuclis observada per microscòpia electrònica durant el pas de nucleació de la precipitació AgBr de dos raigs. Això és molt eficaç quan s'aplica el mètode de quantificació conductomètrica.

Quan es van calcular aquests valors de Script, van prendre γ=140 mJ m - 2. Com que la nucleació en sistemes oberts correspon al procés de supervivència de nuclis naixents creats en una zona local de sobresaturació extremadament alta prop de les sortides dels reactius, és crític. la sobresaturació correspon a la concentració del solut en equilibri amb nuclis de mida màxima, si fem servir les dades de Sugimoto35 sobre el radi màxim dels nuclis d'AgBr en sistemes oberts (.3 8.3 nm) amb γ teòric per a AgBr cúbic (=109 mJ m − 2).) 3, aleshores el factor de sobresaturació crític, Scrit, es calcula com seria 1,36 a 25 °C (si se suposa que γ és 140 mJ/m2, aleshores Scrit=1,48).
En conseqüència, en tot cas, supersaturacions crítiques aEls sistemes oberts de partícules d'halogenur de plata solen estar molt per sota de les sobresaturacions màximes (probablement properes a les sobresaturacions crítiques) en sistemes tancats. Això es deu al fet que el radi mitjà dels nuclis generats a la zona local d'un sistema obert és molt més gran que rmen un sistema tancat, probablement a causa de la fusió instantània de nuclis primaris altament concentrats a la zona local d'un sistema obert amb un alt concentració local d'electròlits.
Aplicació
S'ha estudiat i analitzat àmpliament l'ús del mètode de valoració conductomètrica per a l'enregistrament continu durant els processos enzimàtics. Gairebé tots els mètodes analítics electroquímics es basen en reaccions electroquímiques (potenciometria, voltammetria, amperometria, coulometria).
El mètode d'anàlisi conductomètric és un mètode en què no hi ha reaccions electroquímiques en els elèctrodes, o bé hi ha reaccions secundàries que es poden descuidar. Per tant, en aquest mètode, la propietat més important de la solució d'electròlit a la capa límit és la seva conductivitat elèctrica, que varia segons un rang força ampli de reaccions biològiques.
Avantatges
Els biosensors conductomètrics també tenen alguns avantatges respecte a altres tipus de transductors. En primer lloc, es poden fer amb tecnologia estàndard de pel·lícula fina de baix cost. Això, juntament amb l'ús d'un mètode optimitzat per immobilitzar material biològic, comporta una reducció important tant del cost primari dels dispositius com decost total de l'anàlisi. Per als microbiosensors integrats, és fàcil realitzar el mode de mesura diferencial, que compensa les influències externes i millora considerablement la precisió de la mesura.
Les dades mostren clarament el gran potencial dels biosensors conductomètrics. Tanmateix, aquesta és una tendència força nova en biosensors, de manera que el desenvolupament de dispositius comercials té un futur prometedor.
Mètodes nous
Alguns científics han descrit un mètode general per mesurar pKa per conductància. Aquest mètode va ser àmpliament utilitzat fins al voltant de 1932 (abans que s'utilitzaven els mètodes de mesura de pH). El mètode conductomètric és extremadament sensible a la temperatura i no es pot utilitzar per mesurar valors de pKa superposats. Un possible avantatge per a mostres sense cromòfor és que es pot utilitzar en solucions molt diluïdes, fins a 2,8 × 10-5 M. En els darrers anys s'ha fet servir la conductometria 87 per mesurar el pKa de la lidocaïna, tot i que el resultat obtingut va ser de 0,7. per unitat per sota del valor de pH generalment acceptat.

Albert i Sergeant també van descriure un mètode per determinar el pKa a partir de mesures de solubilitat. Com s'ha esmentat anteriorment, la solubilitat depèn del pKa, de manera que si la solubilitat es mesura a diversos valors de pH en una corba, es pot determinar el pKa. Peck i Benet van descriure un mètode general per estimar els valors de pKa per a substàncies monopròtiques, dipròtiques i amfòteres donades un conjunt de mesures de solubilitat i pH. Hansen i Hafliger van obtenir el pKa de la mostra, quees descompon ràpidament per hidròlisi a partir de les seves taxes de dissolució inicials en funció del pH en un dispositiu de disc giratori. El resultat coincideix bé amb el resultat pH/UV, però la descomposició dificulta aquest darrer mètode. Aquesta és, en general, una descripció del mètode d'anàlisi conductomètric.






