L'estat tridimensional de l'aigua líquida és difícil d'estudiar, però s'ha après molt analitzant l'estructura dels cristalls de gel. Quatre àtoms d'oxigen que interactuen amb l'hidrogen ocupen els vèrtexs d'un tetraedre (tetra=quatre, edre=pla). L'energia mitjana necessària per trencar aquest enllaç en el gel s'estima en 23 kJ/mol-1.

La capacitat de les molècules d'aigua per formar un nombre determinat de cadenes d'hidrogen, així com una força determinada, crea un punt de fusió inusualment alt. Quan es fon, és retingut per aigua líquida, l'estructura de la qual és irregular. La majoria dels ponts d'hidrogen estan distorsionats. Es necessita una gran quantitat d'energia en forma de calor per trencar la xarxa cristal·lina del gel enllaçat per hidrogen.
Característiques de l'aparició del gel (Ih)
Molts dels habitants es pregunten quin tipus de gel cristal·lí té. NecessariCal tenir en compte que la densitat de la majoria de substàncies augmenta durant la congelació, quan els moviments moleculars s'alenteixen i es formen cristalls densament empaquetats. La densitat de l'aigua també augmenta a mesura que es refreda fins a un màxim a 4 °C (277K). Aleshores, quan la temperatura baixa per sota d'aquest valor, s'expandeix.
Aquest augment es deu a la formació d'un cristall de gel obert, enllaçat per hidrogen, amb la seva gelosia i menor densitat, en el qual cada molècula d'aigua està rígidament lligada per l'element anterior i quatre valors més, mentre es mou prou ràpid per tenir més massa. Com que es produeix aquesta acció, el líquid es congela de d alt a baix. Això té importants resultats biològics, com a conseqüència dels quals la capa de gel de l'estany aïlla els éssers vius del fred extrem. A més, dues propietats addicionals de l'aigua estan relacionades amb les seves característiques de l'hidrogen: la calor específica i l'evaporació.
Descripció detallada de les estructures
El primer criteri és la quantitat necessària per augmentar 1 °C la temperatura d'1 gram d'una substància. L'augment dels graus d'aigua requereix una quantitat relativament gran de calor perquè cada molècula està implicada en nombrosos enllaços d'hidrogen que s'han de trencar per tal que l'energia cinètica augmenti. Per cert, l'abundància de H2O a les cèl·lules i teixits de tots els grans organismes pluricel·lulars significa que les fluctuacions de temperatura dins de les cèl·lules es minimitzen. Aquesta característica és crucial, ja que la velocitat de la majoria de reaccions bioquímiquessensible.
La calor de vaporització de l'aigua també és significativament superior a la de molts altres líquids. Es necessita una gran quantitat de calor per convertir aquest cos en gas, perquè s'han de trencar els ponts d'hidrogen per tal que les molècules d'aigua es disloquin entre si i entrin en aquesta fase. Els cossos canviables són dipols permanents i poden interactuar amb altres compostos similars i amb els que s'ionitzen i es dissolen.
Les altres substàncies esmentades anteriorment només poden entrar en contacte si hi ha polaritat. És aquest compost el que intervé en l'estructura d'aquests elements. A més, pot alinear-se al voltant d'aquestes partícules formades a partir d'electròlits, de manera que els àtoms d'oxigen negatius de les molècules d'aigua s'orienten als cations, i els ions positius i els àtoms d'hidrogen s'orienten als anions.
En els sòlids, per regla general, es formen xarxes cristal·lines moleculars i atòmiques. És a dir, si el iode es construeix de tal manera que conté I2, , aleshores en el diòxid de carboni sòlid, és a dir, en el gel sec, les molècules de CO2 són situat als nodes de la xarxa cristal·lina . Quan interacciona amb substàncies similars, el gel té una xarxa cristal·lina iònica. El grafit, per exemple, que té una estructura atòmica basada en carboni, no és capaç de canviar-lo, igual que el diamant.
Què passa quan un cristall de sal de taula es dissol a l'aigua: les molècules polars són atretes pels elements carregats del cristall, la qual cosa provoca la formació de partícules similars de sodi i clorur a la seva superfície, donant lloc a aquests cossoses disloquen l'un de l' altre i comença a dissoldre's. A partir d'aquí es pot observar que el gel té una xarxa cristal·lina amb enllaç iònic. Cada Na + dissolt atreu els extrems negatius de diverses molècules d'aigua, mentre que cada Cl - dissolt atreu els extrems positius. La closca que envolta cada ió s'anomena esfera d'escapament i normalment conté diverses capes de partícules de dissolvent.
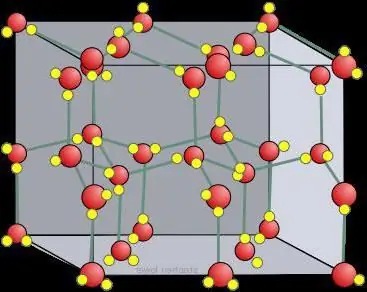
Reticleta de cristall de gel sec
Les variables o un ió envoltat d'elements es diu que estan sulfatades. Quan el dissolvent és aigua, aquestes partícules s'hidraten. Així, qualsevol molècula polar tendeix a ser solvatada pels elements del cos líquid. En el gel sec, el tipus de xarxa cristal·lina forma enllaços atòmics en estat d'agregació, que no canvien. Una altra cosa és el gel cristal·lí (aigua congelada). Els compostos orgànics iònics com la carboxilasa i les amines protonades han de ser solubles en grups hidroxil i carbonil. Les partícules contingudes en aquestes estructures es mouen entre molècules i els seus sistemes polars formen enllaços d'hidrogen amb aquest cos.
Per descomptat, el nombre dels últims grups indicats en una molècula afecta la seva solubilitat, que també depèn de la reacció de diverses estructures de l'element: per exemple, els alcohols d'un, dos i tres carbonis són miscibles. amb aigua, però els hidrocarburs més grans amb compostos hidroxil individuals estan molt menys diluïts en líquids.
Hexagonal Ih té una forma similar axarxa cristal·lina atòmica. Per al gel i tota la neu natural de la Terra, sembla exactament així. Això s'evidencia per la simetria de la xarxa cristal·lina del gel, que es va cultivar a partir del vapor d'aigua (és a dir, dels flocs de neu). Es troba al grup espacial P 63/mm a partir de 194; D 6h, classe Laue 6/mm; similar a β-, que té un múltiple de 6 eixos helicoïdals (rotació al voltant a més de desplaçar-se al llarg). Té una estructura de baixa densitat força oberta on l'eficiència és baixa (~1/3) en comparació amb estructures cúbiques simples (~1/2) o cúbiques centrades en cares (~3/4).
En comparació amb el gel normal, la xarxa cristal·lina del gel sec, unida per molècules de CO2, és estàtica i només canvia quan els àtoms es desintegran.
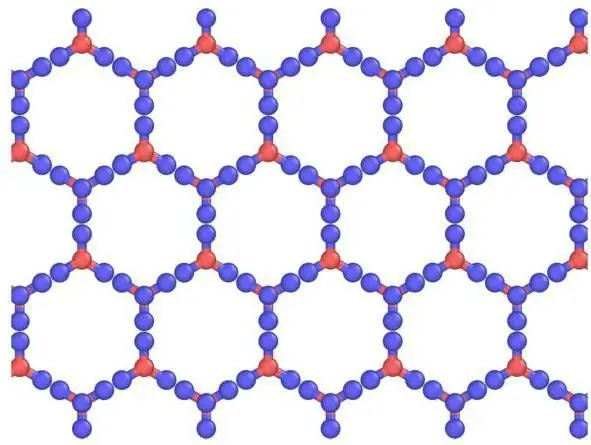
Descripció de les reixes i els seus elements
Els cristalls es poden veure com a models cristal·lins, formats per làmines col·locades una sobre l' altra. L'enllaç d'hidrogen està ordenat, mentre que en realitat és aleatori, ja que els protons poden moure's entre molècules d'aigua (gel) a temperatures superiors a uns 5 K. De fet, és probable que els protons es comportin com un fluid quàntic en un flux de túnel constant. Això es veu millorat per la dispersió dels neutrons, que mostra la seva densitat de dispersió a mig camí entre els àtoms d'oxigen, indicant la localització i el moviment concertat. Aquí hi ha una semblança de gel amb una xarxa cristal·lina atòmica i molecular.
Les molècules tenen una disposició esglaonada de la cadena d'hidrogenrespecte als seus tres veïns de l'avió. El quart element té una disposició d'enllaç d'hidrogen eclipsada. Hi ha una lleugera desviació de la simetria hexagonal perfecta, ja que la cel·la unitat és un 0,3% més curta en la direcció d'aquesta cadena. Totes les molècules experimenten els mateixos entorns moleculars. Hi ha prou espai dins de cada "caixa" per contenir partícules d'aigua intersticial. Encara que no es consideren generalment, recentment s'han detectat eficaçment per difracció de neutrons de la xarxa cristal·lina en pols de gel.
Canvi de substàncies
El cos hexagonal té punts triples amb aigua líquida i gasosa 0,01 ° C, 612 Pa, elements sòlids - tres -21,985 ° C, 209,9 MPa, onze i dos -199,8 ° C, 70 MPa, així com - 34,7 ° C, 212,9 MPa. La constant dielèctrica del gel hexagonal és 97,5.
La corba de fusió d'aquest element ve donada per MPa. Les equacions d'estat estan disponibles, a més d'elles, algunes desigu altats senzilles que relacionen el canvi de propietats físiques amb la temperatura del gel hexagonal i les seves suspensions aquoses. La duresa fluctua amb graus que augmenten des del guix o per sota (≦2) a 0 °C fins a feldspat (6 Mohs) a -80 °C, un canvi anormalment gran en la duresa absoluta (> 24 vegades).
La xarxa cristal·lina hexagonal de gel forma plaques i columnes hexagonals, on les cares superior i inferior són els plans basals {0 0 0 1} amb una entalpia de 5,57 μJ cm -2i altres parts laterals equivalents s'anomenen parts del prisma {1 0 -1 0} amb 5, 94µJ cm -2. Les superfícies secundàries {1 1 -2 0} amb 6,90 ΜJ ˣ cm -2 es poden formar al llarg dels plans formats pels costats de les estructures.
Aquesta estructura mostra una disminució anòmala de la conductivitat tèrmica amb l'augment de la pressió (així com el gel cúbic i amorf de baixa densitat), però difereix de la majoria dels cristalls. Això es deu a un canvi en l'enllaç d'hidrogen, que redueix la velocitat transversal del so a la xarxa cristal·lina de gel i aigua.
Hi ha mètodes que descriuen com preparar mostres grans de cristall i qualsevol superfície de gel desitjada. Se suposa que l'enllaç d'hidrogen a la superfície del cos hexagonal objecte d'estudi estarà més ordenat que a l'interior del sistema a granel. L'espectroscòpia variacional amb generació de freqüències en xarxa de fases ha demostrat que hi ha una asimetria estructural entre les dues capes superiors (L1 i L2) a la cadena H2O subsuperficial de la superfície basal del gel hexagonal. Els enllaços d'hidrogen adoptats a les capes superiors dels hexàgons (L1 O ··· HO L2) són més forts que els acceptats a la segona capa a l'acumulació superior (L1 OH ··· O L2). Estructures de gel hexagonals interactives disponibles.
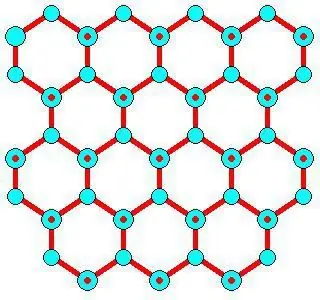
Funcions de desenvolupament
El nombre mínim de molècules d'aigua necessàries per formar gel és d'aproximadament 275 ± 25, com per a un cúmul icosaèdric complet de 280. La formació es produeix a una velocitat de 10 10 al interfície aire-aigua i no en aigua a granel. El creixement dels cristalls de gel depèn de diferents taxes de creixement de diferentsenergies. L'aigua s'ha de protegir de la congelació quan es criopreserven mostres biològiques, aliments i òrgans.
Això s'aconsegueix normalment mitjançant velocitats de refredament ràpides, utilitzant mostres petites i un crioconservador i augmentant la pressió per nuclear gel i prevenir danys cel·lulars. L'energia lliure de gel/líquid augmenta de ~30 mJ/m2 a pressió atmosfèrica a 40 mJ/m-2 a 200 MPa, cosa que indica motiu pel qual es produeix aquest efecte.
Quin tipus de gelosia cristal·lina és característica del gel
Com a alternativa, poden créixer més ràpidament a partir de superfícies prismàtiques (S2), a la superfície alterada aleatòriament de llacs congelats ràpidament o agitats. El creixement de les cares {1 1 -2 0} és almenys el mateix, però les converteix en bases prismàtiques. Les dades sobre el desenvolupament del cristall de gel s'han investigat completament. Les taxes relatives de creixement dels elements de diferents cares depenen de la capacitat de formar un gran grau d'hidratació articular. La temperatura (baixa) de l'aigua circumdant determina el grau de ramificació del cristall de gel. El creixement de les partícules està limitat per la velocitat de difusió a un baix grau de superrefrigeració, és a dir, <2 °C, el que resulta en més.

Però limitat per la cinètica de desenvolupament a nivells més alts de depressió de >4 °C, donant lloc al creixement de l'agulla. Aquesta forma és similar a l'estructura del gel sec (té una xarxa cristal·lina amb una estructura hexagonal), diversescaracterístiques del desenvolupament de la superfície i la temperatura de l'aigua circumdant (sobrerefredada), que hi ha darrere de les formes planes dels flocs de neu.
La formació de gel a l'atmosfera afecta profundament la formació i les propietats dels núvols. Els feldspats, que es troben a la pols del desert que entra a l'atmosfera en milions de tones per any, són formadors importants. Les simulacions per ordinador han demostrat que això es deu a la nucleació de plans de cristalls de gel prismàtics en plans de superfície d' alta energia.
Alguns altres elements i gelosies
Les substàncies dissoltes (a excepció de l'heli i l'hidrogen molt petits, que poden entrar als intersticis) no es poden incloure a l'estructura Ih a pressió atmosfèrica, sinó que són forçades a sortir a la superfície o a la capa amorfa entre les partícules del cos microcristal·lí. Hi ha alguns altres elements als llocs de gelosia del gel sec: ions caotròpics com ara NH4 + i Cl - que s'inclouen a la congelació líquida més lleugera que altres cosmotròpics, com ara Na + i SO42-, de manera que no és possible eliminar-los a causa del fet que formen una fina pel·lícula del líquid restant entre els cristalls. Això pot provocar una càrrega elèctrica de la superfície a causa de la dissociació de l'aigua superficial que equilibra les càrregues restants (que també pot provocar radiació magnètica) i un canvi en el pH de les pel·lícules líquides residuals, per exemple, NH 42SO4 es torna més àcid i el NaCl es torna més bàsic.
Són perpendiculars a les caresxarxa cristal·lina de gel que mostra la següent capa unida (amb àtoms d'O en negre). Es caracteritzen per una superfície basal de creixement lent {0 0 0 1}, on només s'uneixen molècules d'aigua aïllades. Una superfície {1 0 -1 0} de creixement ràpid d'un prisma on parells de partícules recentment unides es poden unir entre si amb hidrogen (un enllaç d'hidrogen/dues molècules d'un element). La cara de creixement més ràpid és {1 1 -2 0} (prismàtica secundària), on les cadenes de partícules recentment unides poden interactuar entre elles mitjançant enllaços d'hidrogen. Una de les seves cadenes/molècules d'element és una forma que forma crestes que divideixen i fomenten la transformació en dos costats del prisma.
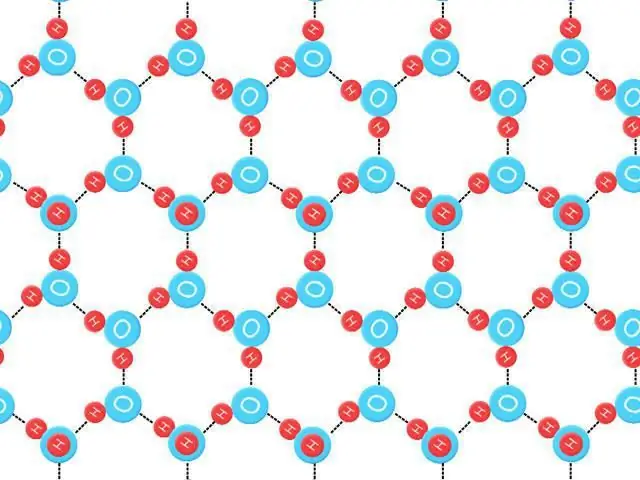
Entropia del punt zero
Es pot definir com S 0=k B ˣ Ln (N E0), on k B és la constant de Boltzmann, NE és el nombre de configuracions a l'energia E i E0 és l'energia més baixa. Aquest valor de l'entropia del gel hexagonal a zero Kelvin no viola la tercera llei de la termodinàmica "L'entropia d'un cristall ideal en zero absolut és exactament zero", ja que aquests elements i partícules no són ideals, tenen enllaços d'hidrogen desordenats.
En aquest cos, l'enllaç d'hidrogen és aleatori i canvia ràpidament. Aquestes estructures no són exactament iguals en energia, però s'estenen a un nombre molt gran d'estats energèticament propers, obeeixen les "regles del gel". L'entropia del punt zero és el desordre que es mantindria encara que el material es pogués refredar a l'absolutzero (0 K=-273, 15 ° C). Genera confusió experimental per al gel hexagonal 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teòricament, seria possible calcular l'entropia zero dels cristalls de gel coneguts amb una precisió molt més gran (sen tenir en compte els defectes i la propagació del nivell d'energia) que determinar-la experimentalment.
Científics i el seu treball en aquesta àrea
Es pot definir com S 0=k B ˣ Ln (N E0), on k B és la constant de Boltzmann, NE és el nombre de configuracions a l'energia E i E0 és l'energia més baixa. Aquest valor de l'entropia del gel hexagonal a zero Kelvin no viola la tercera llei de la termodinàmica "L'entropia d'un cristall ideal en zero absolut és exactament zero", ja que aquests elements i partícules no són ideals, tenen enllaços d'hidrogen desordenats.
En aquest cos, l'enllaç d'hidrogen és aleatori i canvia ràpidament. Aquestes estructures no són exactament iguals en energia, però s'estenen a un nombre molt gran d'estats energèticament propers, obeeixen les "regles del gel". L'entropia del punt zero és el desordre que es mantindria encara que el material es pogués refredar fins al zero absolut (0 K=-273,15 °C). Genera confusió experimental per al gel hexagonal 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teòricament, seria possible calcular l'entropia zero dels cristalls de gel coneguts amb una precisió molt més gran (sen tenir en compte els defectes i la propagació del nivell d'energia) que determinar-la experimentalment.

Tot i que l'ordre dels protons en el gel a granel no està ordenat, la superfície probablement prefereix l'ordre d'aquestes partícules en forma de bandes d'àtoms d'H penjants i parells O-únics (entropia zero amb enllaços d'hidrogen ordenats). Es troba el trastorn del punt zero ZPE, J ˣ mol -1 ˣ K -1 i altres. A partir de tot l'anterior, és clar i comprensible quins tipus de gelosia cristal·lina són característics del gel.






