En els nostres temps, la física s'ha convertit en una ciència molt comuna. És literalment present a tot arreu. L'exemple més elemental: una pomera creix al teu jardí i els fruits maduren, arriba el moment i les pomes comencen a caure, però en quina direcció cauen? Gràcies a la llei de la gravitació universal, el nostre fetus cau a terra, és a dir, baixa, però no cap amunt. Va ser un dels exemples més famosos de la física, però prestem atenció a la termodinàmica, o més precisament, als equilibris de fases, que no són menys importants a la nostra vida.
Termodinàmica

Primer de tot, mirem aquest terme. ΘερΜοδυναΜική - així es veu la paraula en grec. La primera part ΘερΜo significa "calor", i la segona δυναΜική significa "força". La termodinàmica és una branca de la física que estudia les propietats d'un sistema macroscòpic, així com diverses maneres de convertir i transferir energia. En aquest apartat s'estudien especialment diversos estats i processos per tal que el concepte de temperatura es pugui introduir en la descripció (és una magnitud física que caracteritza un sistema termodinàmic i que es mesura mitjançantdeterminats aparells). Tots els processos en curs en sistemes termodinàmics només es descriuen per magnituds microscòpiques (pressió i temperatura, així com la concentració de components).
Equació de Clapeyron-Clausius
Tots els físics coneixen aquesta equació, però anem a desglossar-la peça per peça. Es refereix als processos d'equilibri de la transició de certa matèria d'una fase a una altra. Això es veu clarament en aquests exemples: fusió, evaporació, sublimació (una de les maneres de conservar els productes, que té lloc eliminant completament la humitat). La fórmula mostra clarament els processos en curs:
- n=PV/RT;
- on T és la temperatura de la substància;
- Presió P;
- calor de transició de fase específica de R;
- V-canvi en un volum específic.
La història de la creació de l'equació

L'equació de Clausius-Clapeyron és una excel·lent explicació matemàtica de la segona llei de la termodinàmica. També es coneix com la "desigu altat de Clausius". Naturalment, el teorema va ser desenvolupat pel mateix científic, que volia explicar la relació entre el flux de calor al sistema i l'entropia, així com el seu entorn. Aquesta equació va ser desenvolupada per Clausius en els seus intents d'explicar i quantificar l'entropia. En sentit literal, el teorema ens dóna l'oportunitat de determinar si un procés cíclic és reversible o irreversible. Aquesta desigu altat ens ofereix una fórmula quantitativa per entendre la segona llei.
El científic va ser un dels primers a treballar la idea de l'entropia, i fins i tot la va donarnom del procés. El que ara es coneix com el teorema de Clausius es va publicar per primera vegada l'any 1862 en el sisè treball de Rudolf, Sobre l'ús del teorema d'equivalència de transformació per al treball interior. El científic va intentar mostrar una relació proporcional entre l'entropia i el flux d'energia mitjançant l'escalfament (δ Q) al sistema. En la construcció, aquesta energia tèrmica es pot convertir en treball, i es pot transformar en calor mitjançant un procés cíclic. Rudolph va demostrar que "la suma algebraica de totes les transformacions que es produeixen en un procés cíclic només pot ser inferior a zero o, en casos extrems, igual a zero".
Sistema aïllat tancat
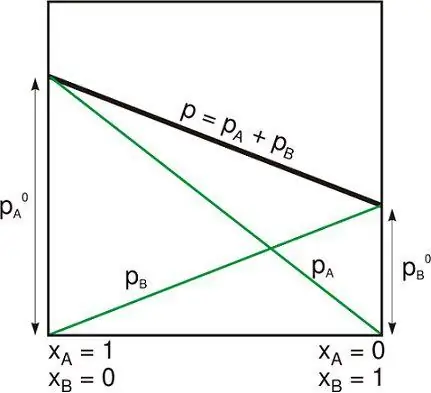
El sistema aïllat és un dels següents:
- El sistema físic està lluny d' altres que no interactuen amb ells.
- El sistema termodinàmic està tancat per parets rígides i immòbils per les quals no poden passar ni matèria ni energia.
Malgrat que el subjecte està relacionat internament amb la seva pròpia gravetat, un sistema aïllat normalment es porta més enllà dels límits de la gravitació externa i d' altres forces distants.
Això es pot contrastar amb el que (en la terminologia més general utilitzada en termodinàmica) s'anomena sistema tancat envoltat de parets selectives a través dels quals es pot transferir energia en forma de calor o treball, però no matèria. I amb un sistema obert en què la matèria i l'energia entra o surt, encara que pot tenir diverses parets impenetrables enparts dels seus límits.
Un sistema aïllat obeeix la llei de conservació. Molt sovint en termodinàmica, la matèria i l'energia es consideren conceptes separats.
Transicions termodinàmiques
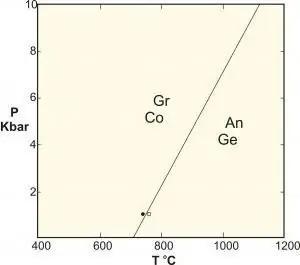
Per entendre les transicions de fase quàntica, és útil comparar-les amb transformacions clàssiques (també anomenades inversions tèrmiques). CPT descriu la cúspide de les propietats termodinàmiques d'un sistema. Indica la reorganització de les partícules. Un exemple típic és la transició de congelació de l'aigua, que descriu una transició suau entre un líquid i un sòlid. Els creixements de fase clàssica es deuen a la competència entre l'energia del sistema i l'entropia de les seves fluctuacions tèrmiques.
Un sistema clàssic no té entropia a temperatura zero i, per tant, no es pot produir cap transformació de fase. El seu ordre està determinat pel potencial termodinàmic de la primera derivada discontínua. I, per descomptat, té el primer ordre. Les transformacions de fase d'un ferroimant a un paraimant són contínues i de segon ordre. Aquests canvis constants d'una fase ordenada a una desordenada es descriuen mitjançant un paràmetre d'ordre que és zero. Per a la transformació ferromagnètica anterior, el paràmetre d'ordre serà la magnetització total del sistema.
Potencial de Gibbs
L'energia lliure de Gibbs és la quantitat màxima de treball sense expansió que es pot treure d'un sistema tancat termodinàmic (que pot intercanviar calor i treballar amb el medi ambient). Talel màxim resultat només es pot obtenir en un procés completament reversible. Quan el sistema torna del primer estat al segon, la reducció de l'energia lliure de Gibbs és igual a la que realitza el sistema en el seu entorn, menys el treball de les forces de pressió.
Estats de saldo

L'equilibri termodinàmic i mecànic és un concepte axiomàtic de la termodinàmica. Aquest és l'estat intern d'un o més sistemes connectats per parets més o menys permeables o impermeables. En aquest estat, no hi ha fluxos macroscòpics purs de matèria o energia, ni dins d'un sistema ni entre sistemes.
En la seva pròpia concepció de l'estat d'equilibri intern, el canvi macroscòpic no es produeix. Els sistemes es troben simultàniament en mutu equilibri tèrmic, mecànic, químic (constant), de radiació. Poden tenir la mateixa forma. En aquest procés, totes les vistes es guarden alhora i indefinidament fins que es trenca el funcionament físic. En equilibri macroscòpic, es produeixen intercanvis equilibrats perfectament precisos. La prova anterior és una explicació física d'aquest concepte.
Nocions bàsiques
Cada llei, teorema, fórmula té els seus propis fonaments. Vegem els 3 fonaments de la llei de l'equilibri de fases.
- La fase és una forma de matèria, homogènia en composició química, estat físic i equilibri mecànic. Les fases típiques són sòlida, líquida i gasosa. Dos líquids immiscibles (o mescles líquides amb diferents composicions) separats per un límit separat es consideren dues fases diferents i sòlids immiscibles.
- El nombre de components (C) és el nombre de components químicament independents del sistema. El nombre mínim d'espècies independents necessaris per determinar la composició de totes les fases del sistema.
- El nombre de graus de llibertat (F) en aquest context és el nombre de variables intensives que són independents entre si.
Classificació per equilibris de fase
- Les reaccions de transferència neta contínua (sovint anomenades reaccions d'estat sòlid) es produeixen entre matèria sòlida de diferent composició. Poden incloure elements que es troben en líquids (H, C), però aquests elements es mantenen en fases sòlides, de manera que no hi ha cap fase líquida implicada com a reactius o productes (H2O, CO2). Les reaccions de transferència sòlida pure poden ser contínues o discontínues, o terminals.
- Els polimòrfics són un tipus especial de reacció en fase sòlida que inclou fases de composició idèntica. Exemples clàssics són les reaccions entre silicats d'alumini cianita-silimanita-andalusita, la conversió de grafit en diamant a alta pressió i l'equilibri del carbonat de calci.
Lleis de l'equilibri

La regla de la fàbrica de Gibbs va ser proposada per Josiah Willard Gibbs en el seu famós document titulat "L'equilibri de les substàncies heterogènies", que va aparèixer entre 1875 i 1878. S'aplica asistemes heterogenis multicomponent no reactius en equilibri termodinàmic i és una igu altat donada:
- F=C-P+2;
- on F és el nombre de graus de llibertat;
- C: nombre de components;
- P - nombre de fases en equilibri termodinàmic entre si.
El nombre de graus de llibertat és el nombre de variables intensives no ocupades. El major nombre de paràmetres termodinàmics, com la temperatura o la pressió, que poden variar simultàniament i arbitràriament sense afectar-se mútuament. Un exemple de sistema d'un component és un amb un sol producte químic pur, mentre que els sistemes de dos components, com ara les mescles d'aigua i etanol, tenen dos components independents. Les transicions de fase típiques (equilibri de fase) són sòlids, líquids i gasos.
Regla de la fase a pressió constant
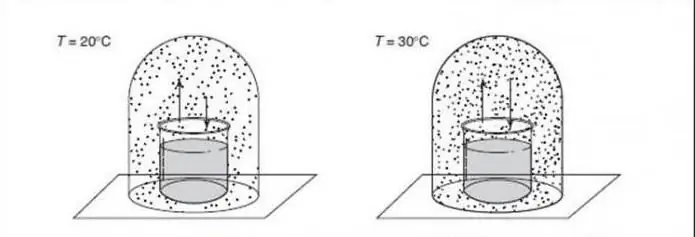
Per a aplicacions en ciència de materials que tracten canvis de fase entre diferents estructures sòlides, sovint es produeix una pressió constant (per exemple, una atmosfera) i s'ignora com a grau de llibertat, de manera que la regla esdevé: F=C - P + 1.
Aquesta fórmula s'introdueix de vegades amb el nom de "regla de la fase condensada", però com sabem, no és aplicable a aquests sistemes sotmesos a altes pressions (per exemple, en geologia), ja que les conseqüències d'aquestes les pressions poden causar conseqüències catastròfiques.
Pot semblar que l'equilibri de fase és només una frase buida, i hi ha pocs processos físics en què aquest momentestà implicat, però, com hem vist, sense ell, moltes de les lleis que coneixem no funcionen, així que cal familiaritzar-se una mica amb aquestes regles úniques, acolorides, encara que una mica avorrides. Aquest coneixement ha ajudat a moltes persones. Van aprendre a aplicar-los a ells mateixos, per exemple, els electricistes, coneixent les regles per treballar amb fases, poden protegir-se d'un perill innecessari.






