Una secció important de la termodinàmica és l'estudi de les transformacions entre diferents fases d'una substància, ja que aquests processos es produeixen a la pràctica i són d'importància fonamental per predir el comportament d'un sistema en determinades condicions. Aquestes transformacions s'anomenen transicions de fase, a les quals està dedicat l'article.
El concepte d'una fase i un component del sistema

Abans de procedir a la consideració de les transicions de fase en física, cal definir el concepte de fase en si. Com se sap pel curs de la física general, hi ha tres estats de la matèria: gasós, sòlid i líquid. En una secció especial de la ciència -en termodinàmica- les lleis es formulen per a les fases de la matèria, i no per als seus estats d'agregació. S'entén per fase un determinat volum de matèria que té una estructura homogènia, es caracteritza per unes propietats físiques i químiques específiques i està separat de la resta de matèria per límits, que s'anomenen interfase.
Així, el concepte de "fase" porta informació molt més pràcticament significativa sobre les propietatsmatèria que el seu estat d'agregació. Per exemple, l'estat sòlid d'un metall com el ferro pot estar en les fases següents: cúbic centrat en el cos magnètic de baixa temperatura (BCC), bcc no magnètic de baixa temperatura, cúbic centrat en la cara (fcc) i cúbic d' alta temperatura. temperatura no magnètica bcc.
A més del concepte de "fase", les lleis de la termodinàmica també utilitzen el terme "components", que significa el nombre d'elements químics que formen un sistema determinat. Això vol dir que la fase pot ser monocomponent (1 element químic) o multicomponent (diversos elements químics).
Teorema de Gibbs i equilibri entre fases del sistema

Per entendre les transicions de fase, cal conèixer les condicions d'equilibri entre elles. Aquestes condicions es poden obtenir matemàticament resolent el sistema d'equacions de Gibbs per a cadascuna d'elles, suposant que s'arriba a l'estat d'equilibri quan l'energia total de Gibbs del sistema aïllat de la influència externa deixa de canviar.
Com a resultat de resoldre el sistema d'equacions indicat, s'obtenen condicions per a l'existència d'equilibri entre diverses fases: un sistema aïllat deixarà d'evolucionar només quan les pressions, potencials químics de cada component i temperatures en totes les fases. són iguals entre si.
Regla de fase de Gibbs per a l'equilibri

Un sistema que consta de diverses fases i components pot estar en equilibri no noméssota determinades condicions, per exemple, a una temperatura i pressió específiques. Algunes de les variables del teorema de Gibbs per a l'equilibri es poden canviar mantenint tant el nombre de fases com el nombre de components que es troben en aquest equilibri. El nombre de variables que es poden canviar sense pertorbar l'equilibri del sistema s'anomena nombre de llibertats d'aquest sistema.
El nombre de llibertats l d'un sistema que consta de f fases i k components es determina de manera única a partir de la regla de fase de Gibbs. Aquesta regla s'escriu matemàticament de la següent manera: l + f=k + 2. Com es treballa amb aquesta regla? Molt simple. Per exemple, se sap que el sistema consta de f=3 fases d'equilibri. Quin és el nombre mínim de components que pot contenir un sistema d'aquest tipus? Podeu respondre la pregunta raonant de la següent manera: en el cas de l'equilibri, les condicions més estrictes existeixen quan només es realitza amb determinats indicadors, és a dir, un canvi en qualsevol paràmetre termodinàmic conduirà a un desequilibri. Això vol dir que el nombre de llibertats l=0. Substituint els valors coneguts de l i f, obtenim k=1, és a dir, un sistema en què tres fases estan en equilibri pot constar d'un component. Un bon exemple és el punt triple de l'aigua, on el gel, l'aigua líquida i el vapor existeixen en equilibri a temperatures i pressions específiques.
Classificació de les transformacions de fase
Si comenceu a canviar alguns paràmetres termodinàmics en un sistema en equilibri, podeu observar com una fase desapareixerà i n'apareix una altra. Un exemple senzill d'aquest procés és la fusió del gel quan s'escalfa.
Atès que l'equació de Gibbs depèn només de dues variables (pressió i temperatura), i la transició de fase implica un canvi en aquestes variables, aleshores matemàticament la transició entre fases es pot descriure diferenciant l'energia de Gibbs respecte a la seva les variables. Va ser aquest enfocament el que va utilitzar el físic austríac Paul Ehrenfest el 1933, quan va compilar una classificació de tots els processos termodinàmics coneguts que es produeixen amb un canvi en l'equilibri de fase.
De les bases de la termodinàmica es dedueix que la primera derivada de l'energia de Gibbs respecte a la temperatura és igual al canvi en l'entropia del sistema. La derivada de l'energia de Gibbs respecte a la pressió és igual al canvi de volum. Si, quan canvien les fases del sistema, l'entropia o el volum pateix una ruptura, és a dir, canvien bruscament, aleshores es parla d'una transició de fase de primer ordre.
A més, les segones derivades de l'energia de Gibbs pel que fa a la temperatura i la pressió són la capacitat calorífica i el coeficient d'expansió volumètrica, respectivament. Si la transformació entre fases va acompanyada d'una discontinuïtat en els valors de les magnituds físiques indicades, es parla d'una transició de fase de segon ordre.
Exemples de transformacions entre fases

Hi ha un gran nombre de transicions diferents a la natura. En el marc d'aquesta classificació, exemples cridaners de transicions de primer tipus són els processos de fusió de metalls o la condensació del vapor d'aigua de l'aire, quan hi ha un s alt de volum en el sistema.
Si parlem de transicions de segon ordre, llavors exemples sorprenents són la transformació del ferro d'un estat magnètic a un estat paramagnètic a una temperatura768 ºC o la transformació d'un conductor metàl·lic en un estat superconductor a temperatures properes al zero absolut.
Equacions que descriuen transicions del primer tipus
A la pràctica, sovint és necessari conèixer com canvien la temperatura, la pressió i l'energia absorbida (alliberada) en un sistema quan es produeixen transformacions de fase en ell. Amb aquesta finalitat s'utilitzen dues equacions importants. S'obtenen a partir dels coneixements bàsics de la termodinàmica:
- Fórmula de Clapeyron, que estableix la relació entre pressió i temperatura durant les transformacions entre diferents fases.
- Fórmula de Clausius que enllaça l'energia absorbida (alliberada) i la temperatura del sistema durant la transformació.
L'ús d'ambdues equacions no és només per obtenir dependències quantitatives de magnituds físiques, sinó també per determinar el signe del pendent de les corbes d'equilibri en diagrames de fases.
Equació per descriure transicions del segon tipus

Les transicions de fase de 1r i 2n tipus es descriuen per equacions diferents, ja que l'aplicació de les equacions de Clausius i Clausius per a transicions de segon ordre condueix a incertesa matemàtica.
Per descriure aquest últim, s'utilitzen les equacions d'Ehrenfest, que estableixen una relació entre els canvis de pressió i temperatura mitjançant el coneixement dels canvis en la capacitat calorífica i el coeficient d'expansió volumètrica durant el procés de transformació. Les equacions d'Ehrenfest s'utilitzen per descriure transicions conductor-superconductor en absència de camp magnètic.
Importànciadiagrames de fase
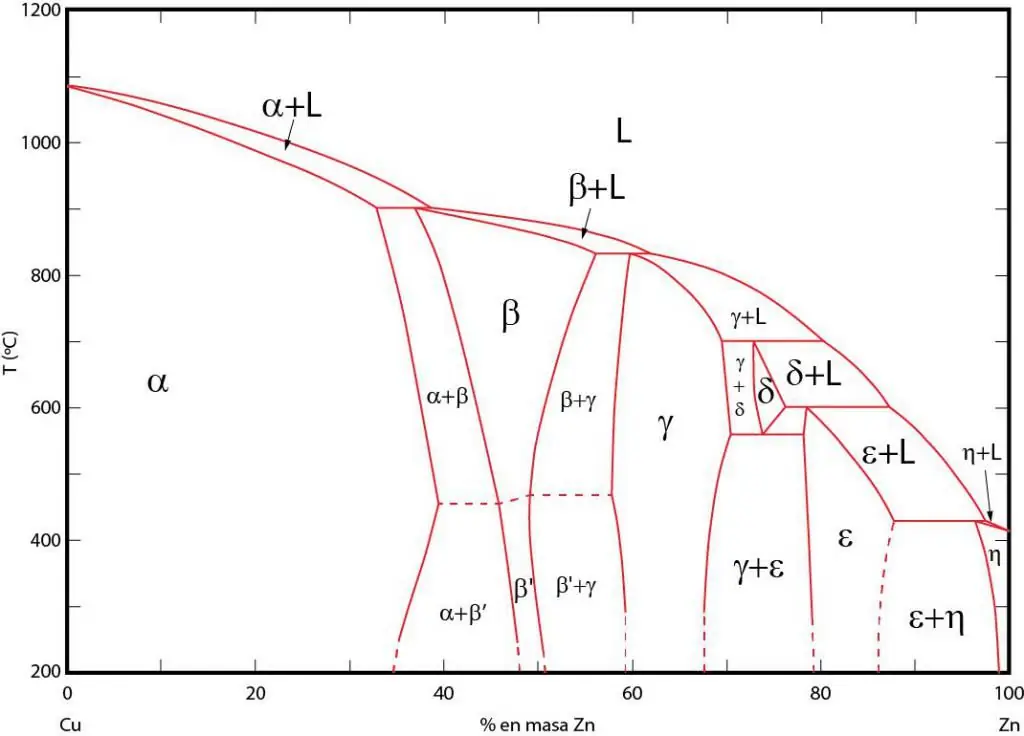
Els diagrames de fases són una representació gràfica d'àrees en què les fases corresponents existeixen en equilibri. Aquestes zones estan separades per línies d'equilibri entre les fases. Sovint s'utilitzen diagrames de fase P-T (pressió-temperatura), T-V (temperatura-volum) i P-V (pressió-volum).
La importància dels diagrames de fase rau en el fet que permeten predir en quina fase estarà el sistema quan les condicions externes canviïn en conseqüència. Aquesta informació s'utilitza en el tractament tèrmic de diversos materials per tal d'obtenir una estructura amb les propietats desitjades.






